La influencia legislativa de la industria farmacéutica II:
Medicamentos con o sin marca: Los millones en juego
Publicado: 28.11.2013
 La segunda parte de esta serie sobre el lobby en la Ley de Fármacos muestra el juego de intereses de los distintos actores de la industria cuando se trata de vender medicamentos genéricos o de marca. Muchos de los argumentos de los privados se impusieron y obligaron al gobierno a resignarse a una salida intermedia. Finalmente los médicos deberán incluir el nombre genérico de los medicamentos sólo cuando exista una versión certificada de que son igualmente efectivos que los de marca.
La segunda parte de esta serie sobre el lobby en la Ley de Fármacos muestra el juego de intereses de los distintos actores de la industria cuando se trata de vender medicamentos genéricos o de marca. Muchos de los argumentos de los privados se impusieron y obligaron al gobierno a resignarse a una salida intermedia. Finalmente los médicos deberán incluir el nombre genérico de los medicamentos sólo cuando exista una versión certificada de que son igualmente efectivos que los de marca.
Una persona puede ahorrar entre 70 mil y 2,5 millones de pesos al año si compra un remedio bioequivalente en lugar de preferir uno de marca, según un sondeo del Ministerio de Salud que comparó precios en 12 medicamentos. El ahorro se explica por las diferencias de precio, que pueden llegar al 1.600% en el caso de una droga inmunosupresora. El estudio coincide con una agresiva campaña publicitaria del gobierno en los medios que, bajo el eslogan “Elige medicamentos bioequivalentes”, promueve el uso de fármacos genéricos, que están certificados por su eficacia terapéutica. La ofensiva gubernamental ocurre justo cuando el Congreso está a punto a aprobar la nueva Ley de Fármacos que obligará a los médicos a escribir en la receta el nombre genérico del medicamento con bioequivalencia acreditada. La apuesta es que bajen los precios, pero eso está por verse.

Comisión Mixta de fármacos
El camino para llegar a esta fórmula fue pedregoso por el fuerte lobby que ejercieron laboratorios farmacéuticos y cadenas de farmacias en el trabajo legislativo. Ambos defienden un negocio que les renta ganancias en conjunto por un monto superior a los US$2.500 millones al año, y donde la defensa de sus marcas es prioritaria ante la amenaza de que se extienda el mercado de los genéricos bioequivalentes con precios más competitivos. CIPER reconstruyó la ruta del lobby en el trabajo parlamentario en un punto altamente sensible para la industria: la regulación de incentivos y la definición de los genéricos bioequivalentes en la receta médica.
Así como las farmacias marcaron presencia a lo largo de toda la tramitación del proyecto en la Cámara de Diputados, los laboratorios farmacéuticos y distribuidores hicieron pesar su opinión en reiteradas ocasiones en las comisiones a través de José Manuel Cousiño, vicepresidente ejecutivo de la Cámara de la Innovación Farmacéutica de Chile (CIF); y de Sergio Cedano, Elmer Torres y Rodrigo Cabello, presidente, gerente general y asesor legislativo de la Asociación de Industriales de Farmacias (ASILFA); además de Jorge Velis, director ejecutivo de la Cámara de Medicamentos de Venta Directa (Cameved).
A diferencia del Senado, que publica en su página web quiénes asisten a cada sesión, en la Cámara de Diputados no hay obligación de registrarse como público al trabajo de comisiones. Y es allí, según testimonios recogidos, donde se despliega otra de las estrategias de los lobbystas. Un parlamentario relató a CIPER:
-Es frecuente que, a través de papelitos, se sugieran ciertos temas de conversación o se propongan determinadas indicaciones. Por ejemplo, te proponen preguntas para hacerle a un invitado determinado. Yo recojo el papel y lo rompo públicamente. Es un insulto a la inteligencia.
En Chile, no existe ninguna posibilidad de saber cuánto dinero destina la industria farmacéutica al ejercicio del lobby. No existe ley que exija transparentar ese gasto. En cambio, en Estados Unidos, se sabe que la industria farmacéutica es la que invierte más dinero en la actividad del lobby. De hecho, la gran reforma sanitaria que impulsó el presidente Obama (“Obamacare”) debió sortear grandes embates del lobby farmacéutico. Según una columna publicada en el diario El País, una congresista estadounidense admitió que, para aprobar el grueso de la ley, debieron ceder a la presión farmacéutica y dejar fuera la posibilidad de que el sistema de salud público Medicare utilizara su poder adquisitivo para regular y de ese modo bajar los precios de los medicamentos.
“EL GOBIERNO HA EJERCIDO LOBBY A FAVOR DE LABORATORIOS”
En este potente lobby cruzado que se desplegó en torno al proyecto de ley de fármacos coincidieron los intereses de los supermercados con los laboratorios farmacéuticos, representados por la CIF y ASILFA. Ambos sectores pujaron para promover la venta abierta de medicamentos sin receta, disputando el dominio a las farmacias en un mercado de US$350 millones anuales.
-Los laboratorios cuentan con el gobierno como socio, el que ha realizado el lobby más grande de la historia republicana del país -acusa el presidente de las farmacias independientes, Héctor Rojas.

Héctor Rojas, representante de las farmacias independientes.
El interés de los laboratorios -especialmente los de innovación- en el nicho de los medicamentos sin receta, tiene una potente explicación: representan una alternativa de reconversión en momentos en que están venciendo las patentes que les permiten fabricar en exclusividad los medicamentos de prescripción médica. Para el año 2015 se prevé que el 87% de los productos farmacéuticos en Estados Unidos serán genéricos y, por lo tanto, con menores retornos económicos porque son más baratos (según antecedentes entregados en la Comisión de Hacienda de la Cámara). De allí que los laboratorios necesiten buscar nuevas alternativas de rentabilidad en los OTC y contar con mayor cantidad de puntos de venta.
-Para esta nueva forma de comercialización, lo que necesitan los laboratorios en Chile es pasar de 1.500 puntos de venta a 15.000 aproximadamente. Este es el verdadero objeto de la insistencia de aprobar esta iniciativa y no una real necesidad de la población -sostiene Héctor Rojas, representante de las farmacias independientes.
Ni el lobby de la industria ni el gobierno pudieron con la mayoría parlamentaria que se opuso a permitir la venta de medicamentos sin receta (OTC) en supermercados y otras tiendas. Esa batalla, al menos, la perdieron.
EL LOBBY DE ZALIASNIK
El segundo nudo de conflicto en la ley de fármacos está en las normas que ponen atajo a las relaciones contaminadas por incentivos entre laboratorios, médicos, visitadores médicos, farmacias y vendedores. Los cambios que vienen son grandes. Allí está el origen de por qué la industria del rubro se ha desplegado en el Congreso. El senador (UDI) Gonzalo Uriarte, admite: “Hay bastante presión. Hay intereses de grandes empresas de por medio, pero nosotros no nos perdemos en procurar el bien común de la población, más allá del interés de las industrias farmacéuticas, de los grupos gremiales y de las grandes empresas”.
En ese contexto, la presencia del abogado Gabriel Zaliasnik durante el trámite del proyecto en comisiones, ha sido motivo de múltiples comentarios entre los parlamentarios. Asistió como invitado a la comisión de salud para dar su “opinión personal” sobre la ley de fármacos, pero de acuerdo a las actas públicas de la sesión, no explicitó que él forma parte del staff de abogados permanentes que asesora al Laboratorio Recalcine. Esta empresa figura entre los principales laboratorios en el país, los que concentran el 47% de los ingresos totales del sector (junto a Laboratorios Chile, Saval, Andrómaco, Pfizer, Merck Serono y Bayer, entre otros).

Gabriel Zaliasnik
Zaliasnik aseguró a CIPER que “lo primero que hice fue decir que si bien tengo un interés personal en el tema por una experiencia familiar en materia de salud, debía dejar constancia que era abogado de laboratorios, hecho por lo demás público y notorio. Tengo interés personal en el tema porque soy abogado especializado en salud, tema que he estudiado en profundidad en Chile y el extranjero a raíz de una enfermedad familiar. Eso es público y conocido. También lo es que como oficina de abogados, somos especialistas en salud y, por lo mismo, trabajamos como abogados para varias empresas e instituciones del área de la salud”.
La prueba más elocuente del compromiso de Zaliasnik con los intereses de los laboratorios es una minuta privada que envió a un grupo de parlamentarios -y a la que accedió CIPER- donde marca puntos que coinciden con los intereses de la industria de los laboratorios. Bajo el encabezado “Postura nuestra finalmente…”, figura mantener la potestad del médico para recetar el medicamento que estime conveniente, y no permitir que en la farmacia se le intercambie por cualquier medicamento, sólo los genéricos bioequivalentes debidamente certificados. Textualmente señala: “Esto para DESEMPODERAR A LAS FARMACIAS…El respeto a la receta médica sirve de contrapeso al poder de la farmacia, impidiendo que ésta reemplace un medicamento por otro de una marca propia o de un laboratorio que proporcione ventajas comerciales a la farmacia en desmedro del paciente” (ver minuta). El abogado Zaliasnik dijo que la minuta fue “abierta y la envié sin distinciones a distintos diputados”.
Los diputados y senadores consultados por CIPER coinciden en que, dentro de las estrategias de lobby, es habitual recibir minutas. Y respecto de este proyecto de ley, señalaron haber recibido documentos con observaciones sobre el proyecto y hasta “indicaciones redactadas” para que los parlamentarios las presentaran como iniciativa personal.
LOS GENÉRICOS PARA BAJAR PRECIOS
Gabriel Zaliasnik y los representantes gremiales de los laboratorios defendieron con ahínco la libertad de los médicos para prescribir el medicamento que estimen conveniente, apuntando a las marcas patentadas o aquellas de genéricos de marca. El argumento es que no se puede cambiar un medicamento patentado o de marca por otro genérico que no tenga reconocida bioequivalencia y que además, este proceso de certificación en Chile no siempre cumple adecuadamente con las normas internacionales. Se opusieron entonces a los cambios.
El proyecto que aprobó el Senado obligaba al médico a prescribir el nombre genérico, conocido como denominación común internacional además de la marca comercial, para que sea el paciente el que baraje alternativas y tengan opciones de intercambiar en la farmacia por un producto más económico, que contenga “el principio activo, dosis y forma farmacéutica recetada”. No se hablaba en ese artículo de exigir bioequivalencia. La Cámara, con el respaldo de la “bancada blanca”, se opuso a intercambiar el medicamento por cualquier genérico y suavizó el texto dejándola como opcional: sólo si el médico lo estima conveniente prescribe el genérico. Este fue el punto que finalmente zanjó la comisión mixta con aprobación unánime de sus miembros, el martes 19 de noviembre. En definitiva, el médico está obligado a prescribir en la receta en nombre genérico, de denominación común internacional, cuando exista bioequivalencia certificada, asegurando además que las farmacias dispongan de un listado mínimo de fármacos para evitar que privilegien determinadas marcas.

Estudio comparativo del MINSAL sobre medicamentos bioequivalentes
Esta decisión importa muchos millones de dólares para el negocio farmacéutico. Facilitar la sustitución del medicamento por un genérico implica un golpe a las marcas –las que tienen patente, las segundas marcas y las de marca propia de farmacias- que generan los mayores ingresos a las cadenas y laboratorios. En el caso de las farmacias, los ingresos que más han aumentado en los últimos cinco años son aquellos generados por los medicamentos de marca propia (100% de aumento). Los genéricos representan el menor crecimiento de ingresos, aun cuando su precio ha crecido en un 40% (ver estudio del Ministerio de Economía).
El último estudio presentado por el Ministerio de Salud, en noviembre de 2013, indica que existen grandes posibilidades de ahorro para la población, al elegir medicamentos bioequivalentes en lugar de los de marca. Las mayores diferencias se producen con el fármaco tacrolimus, que se administra post trasplante de órganos. El ahorro anual alcanza los $2.518.620; la Atorvastatina, que se utiliza para combatir el colesterol alto, implica un ahorro anual para el paciente de $258.216, si se elige el medicamento bioequivalente.
Según datos aportados por el Instituto de Salud Pública (ISP), un 38% de los medicamentos que han sido certificados como bioequivalentes son genéricos de uso habitual. Sin embargo, eso no asegura el acceso de las personas a los medicamentos. Según una encuesta del Sernac de marzo de 2013, sólo el 29,2% de los 131 medicamentos genéricos bioequivalentes aprobados hasta ese momento por el Instituto de Salud Pública (ISP), estaban disponibles en las tres cadenas de farmacias. La diferencia de precios puede alcanzar hasta $34.440 (3.344%) entre productos destinados al tratamiento de la Hipercolesterolemia y de $19.780 (1.009%) en productos destinados a la Hipertensión Arterial, siendo estas patologías frecuentes en la población y en el último caso la primera causa de muerte en Chile (ver estudio Sernac). A partir de agosto de 2013, los medicamentos con bioequivalencia demostrada tienen un sello amarillo con una letra B en el envase, que los hace fácilmente identificables para las personas.
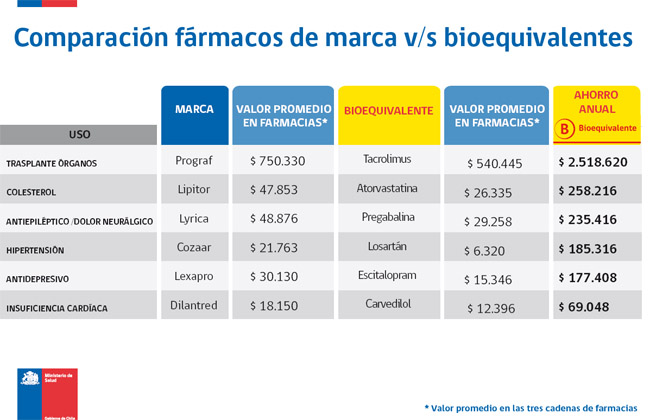
Estudio comparativo del MINSAL sobre medicamentos bioequivalentes
Los laboratorios farmacéuticos no quieren perder terreno con sus marcas (sean patentadas o similares cuando lo fabrican laboratorios distintos al dueño de la patente). Además, deben lidiar con marcas potenciadas por las cadenas farmacéuticas que han ido ganando espacio. Para defender su posición, argumentan que la bioequivalencia que certifica el ISP no garantiza que los medicamentos cumplan con la eficacia terapéutica y los estándares internacionales de buenas prácticas de manufactura. En el Ministerio de Salud responden que hoy existen nueve laboratorios instalados que cumplen todas las normas sobre manufactura para demostrar bioequivalencia, además de veinte agencias que están certificadas bajo las normas internacionales para otorgar el sello de bioequivalencia.
Actualmente existen 283 medicamentos certificados con bioequivalencia, pero el objetivo es cubrir unos 2.000 medicamentos que son los más comercializados dentro del listado general que autoriza el ISP. El costo para certificar un medicamento es de $60 millones aproximadamente y lo debe cancelar el laboratorio respectivo. En la otra cara, tener más bioequivalentes a la venta significaría abrir un gran abanico de opciones para la población, con beneficios económicos directos.
El abogado de Recalcine, Gabriel Zaliasnik, ha sido especialmente activo en la crítica pública al sistema de certificación de bioequivalencia que opera en Chile. Pero insiste en desmarcarse de la actividad del lobby: “Trabajamos como abogados y por lo mismo no hacemos lobby para nadie. Discrepar con la posición del ministro Mañalich no es lobby. Cualquier acusación de lobby solo busca distraer el foco de atención de lo principal, que es la discusión que se está realizando en el Congreso y a quién beneficia la posición de cada uno. ¿Por qué el ministro esconde que los remedios no tienen certificación internacional para ser intercambiables y que los laboratorios de las farmacias son los grandes beneficiados? Creo que la ley de fármacos lisa y llanamente es mala, y que es preocupante la existencia de algunos grupos de interés cuyo financiamiento se desconoce, pero que sí realizan lobby para el ministro Mañalich y que desinforman a la ciudadanía”, aseguró a CIPER.
El alto impacto que tendría en la población la entrada al mercado de medicamentos genéricos con bioequivalencia quedó graficado en un estudio que la Fiscalía Nacional Económica (FNE) dio a conocer en septiembre de 2013, donde se afirma que es la mejor forma de aumentar la competencia y reducir las distorsiones del mercado farmacéutico. Y se estima que puede lograrse hasta un 50% de reducción en los precios de los genéricos, cuando entra al mercado una segunda marca (ver informe).
Facilitar el acceso a medicamentos más baratos es un tema urgente y lo avalan las cifras entregadas por la Organización para la Cooperación y el Desarrollo (OECD). En su último informe sobre la salud 2013, las familias chilenas son las que más gastan en este ámbito, superando a los 34 países miembros. El gasto familiar es de un 4,5% del presupuesto mensual, en el caso de Chile, mientras el promedio se sitúa en un 2,8%. Esta es una cifra elocuente, considerando que además, la mitad de ese gasto se destina a medicamentos, uno de los nudos de proyecto de ley.
En esta discusión, la presencia de la industria fue muy activa, en los pasillos y en comisiones. Según el registro disponible de la Comisión de Salud del Senado, figuran con regularidad como invitados: Fernando del Puerto y Hernan Pfeifer, presidente y vicepresidente de ASILFA; Erick Viertel y Jean-Jacques Duhart, vicepresidente y vicepresidente ejecutivo de la Cámara de la Innovación Farmaceutica (CIF) y la asesora, Asunción Martínez. Por Farmacias Salcobrand, asistió el fiscal Alberto Novoa Pacheco y su asesor, el director de la empresa de comunicaciones Tironi y Asociados, Manuel Melero Abaroa (hermano del diputado UDI y presidente de la Cámara, Patricio Melero). Por Farmacias Cruz Verde figura su director Jorge Brenner Hernández y el asesor Luis Fernando Laso. Además, aparece en el listado sin precisar a quien representó, Carmen Celedón Cariola, socia fundadora de la empresa Imaginacción Asuntos Públicos (que dirige Enrique Correa), la que ha reconocido que Cruz Verde es uno de sus clientes.
 La disputa fue áspera no sólo entre farmacias y laboratorios, sino también al interior de las dos agrupaciones gremiales: CIF y ASILFA. José Manuel Cousiño separó aguas aclarando que los laboratorios de innovación (que tienen patentes) apoyan que los médicos indiquen en la receta el nombre genérico según la denominación común internacional, no así de los productos genéricos de marca (que producen los laboratorios de ASILFA y las farmacias con laboratorios integrados), porque “constituyen una ficción creada por estrategias de marketing y un abuso considerable”. Y graficó lo dicho afirmando que un genérico de denominación común internacional tiene en Chile un precio promedio de US$ 0,80, mientras que uno de marca gira en torno a US$ 5,60, siendo el mismo producto.
La disputa fue áspera no sólo entre farmacias y laboratorios, sino también al interior de las dos agrupaciones gremiales: CIF y ASILFA. José Manuel Cousiño separó aguas aclarando que los laboratorios de innovación (que tienen patentes) apoyan que los médicos indiquen en la receta el nombre genérico según la denominación común internacional, no así de los productos genéricos de marca (que producen los laboratorios de ASILFA y las farmacias con laboratorios integrados), porque “constituyen una ficción creada por estrategias de marketing y un abuso considerable”. Y graficó lo dicho afirmando que un genérico de denominación común internacional tiene en Chile un precio promedio de US$ 0,80, mientras que uno de marca gira en torno a US$ 5,60, siendo el mismo producto.
El ministro Mañalich aportó otra cifra: “La gran utilidad que han hecho las farmacias de cadena ha sido fabricar medicamentos con nombre propio, privilegiando su venta. Las marcas propias desde 2009 han aumentado su venta en 26%, medicamentos que en promedio son cuatro o cinco veces más caros que los genéricos”. Alberto Novoa, fiscal de Salcobrand, replica: “El grupo Salcobrand tiene un laboratorio de muy buen desempeño que vende también sus productos a la competencia y a farmacias independientes. El problema es que sus medicamentos son muy baratos, de modo que cuando la gente pide el producto más económico, inevitablemente llega al de Medipharm”.
EL FIN DE LA “CANELA”
El ministro Jaime Mañalich, ex director de la Clínica Las Condes, sabe bien que esta nueva ley de fármacos quiebra un sistema de incentivos y regalías que hasta ahora operó sin regulación en la cadena de distribución y venta de medicamentos. Por eso, desplegó su furia contra el lobby farmacéutico al que calificó como la “mayor ofensiva” de la industria en el Congreso.

Ministro de Salud, Jaime Mañalich
Un reportaje de Carola Fuentes para el programa Informe Especial de TVN, demostró las variadas formas de marketing que usan los laboratorios farmacéuticos para introducir sus marcas en el mercado: captura con regalos a alumnos de medicina, financiamiento de actividades de formación y de estudios científicos de médicos (“formación continua”), para fidelizarlos con sus marcas, entre otras.
Eso es precisamente lo que la nueva ley pretende eliminar al prohibir cualquier tipo de incentivo “pago, regalo, servicio o beneficio económico entregado o realizado (…) por parte de laboratorios farmacéuticos, droguerías, importadores o distribuidores de medicamentos, establecimientos farmacéuticos en general o por quienes los representen”.
En esa cadena de incentivos, la receta médica es un eslabón esencial: lo que prescribe el médico condiciona mucho la venta. Al terminar con ese condicionante, la nueva ley no sólo fulmina la práctica de los incentivos o “canela” a los vendedores, sino que, además, abre la venta directa de medicamentos en góndolas, lo que pone fin al vendedor intermediario.
Ambos puntos son resistidos por los químicos farmacéuticos y los trabajadores de las farmacias, porque impactan sus ingresos y les resta poder sobre la decisión de compra. Y así lo hicieron también sentir en el Congreso sus representantes, en el trabajo de comisiones y en conversaciones bilaterales con parlamentarios.
Mauricio Acevedo, presidente del sindicato que agrupa a todos los trabajadores de las grandes farmacias, admitió que el sueldo de sus representados tiene un 40% de componente variable y que las mayores comisiones la reciben por la venta de productos de marca propia de la cadena farmacéutica. A cambio de aceptar el fin de los incentivos, los dirigentes lograron –a través de un lobby activo- convencer a los parlamentarios de ambas cámaras de agregar un artículo transitorio a la ley: les asegura un piso mínimo de ingresos, calculado sobre la base de los mejores años de la industria (2011 y 2012), mientras se produce el ajuste de los contratos.
Finalmente, el gobierno no consiguió su propósito de incorporar al retail en la venta de OTC. Lo que sí logró fue que se aprobara la venta en góndolas. Eso significa sacar fuera del mostrador de las farmacias los medicamentos, transparentar más el sistema, de modo que la persona pueda elegir entre más alternativas y cotizar precios, lo que hoy no es posible porque la venta está mediada por el vendedor, motivado a recomendar determinadas marcas por las comisiones que recibe.
Pero no hay buenos augurios para lo que viene. Los trabajadores del rubro ya han advertido: “El riesgo es que la farmacia siga controlando el tema, poniendo en góndola sólo las marcas que les interesan a ellos, y no todas las disponibles en el mercado”. Y las farmacias reclaman que es necesaria la custodia de los químicos farmacéuticos en el puesto de venta y se oponen a la venta directa, a pesar de que esos mismos profesionales reconocen que, en la práctica, están destinados a labores más administrativas del negocio.
Después de tres años de discusión y del despliegue de un lobby que provocó acusaciones inéditas en el Congreso y una disputa destemplada entre quienes se disputan el botín de los fármacos, la ley que pretende regular el sector finalmente llega a su fin. Sólo falta afinar los últimos detalles en comisión mixta y que los acuerdos sean ratificados por ambas cámaras. Antes de fin de año, debiera entrar en vigencia la nueva ley que regula el acceso a los medicamentos en Chile.
FUENTE: CIPERCHILE

No hay comentarios:
Publicar un comentario